Нанороботы нацеливаются на клетки рака молочной железы
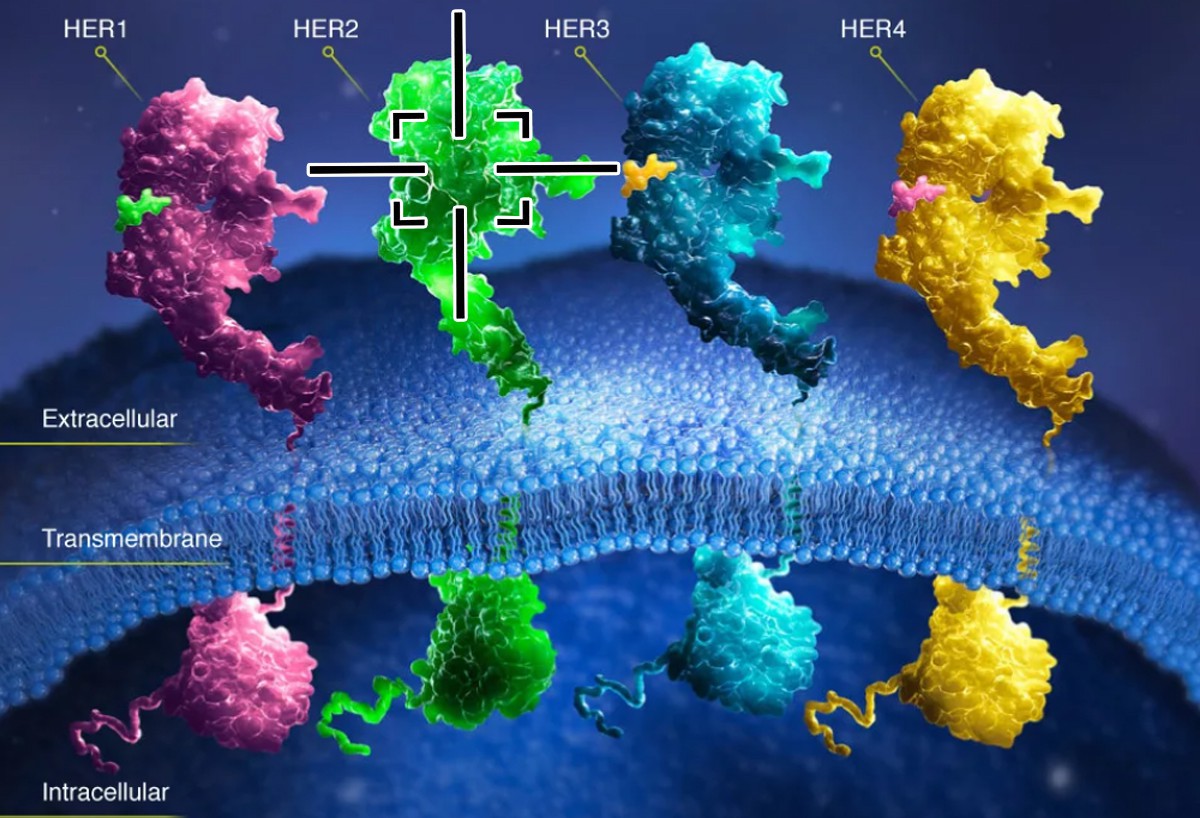
По данным клиники Майо (США), около 20% случаев рака молочной железы связаны с выработкой аномально высокого уровня белка HER2 (второй рецептор фактора роста эпидермиса). Находясь на поверхности раковых клеток, этот сигнальный белок помогает им бесконтрольно размножаться, и связан с плохим прогнозом течения болезни. Исследователи из Сычуаньского университета (КНР) разработали ДНК-наноробота, который распознает HER2 на клетках рака молочной железы, и направляется на их уничтожение.
Современные методы лечения HER2-положительного рака молочной железы включают моноклональные антитела, такие как трастузумаб, которые связываются с HER2 на клетках и направляют его в лизосомы - органеллы, которые разрушают биомолекулы. Снижение уровня HER2 замедляет пролиферацию раковых клеток и запускает их гибель. Но, хотя моноклональные антитела могут привести к гибели раковых клеток, они имеют серьезные побочные эффекты и они дороги. В предыдущем исследовании китайские учёные идентифицировали короткую последовательность ДНК, называемую аптамером, которая распознает и связывает HER2, направляя его на лизосомную деградацию так же, как это делают моноклональные антитела. Но аптамер был не очень стабилен в сыворотке. Теперь исследователи решили добавить к аптамеру наноструктуру ДНК, которая называется тетраэдрической "каркасной" нуклеиновой кислотой (tFNA, tetrahedral framework nucleic acid), и проверить, повысится ли биостабильность аптамера и его противораковая активность.
Чтобы выяснить это, команда создала ДНК-нанороботы, состоящие из tFNA с прикрепленным аптамером HER2. При введении мышам нанороботы сохранялись в кровотоке более чем в два раза дольше, чем свободный аптамер. Затем исследователи добавили нанороботов к трем клеточным линиям рака молочной железы в чашках Петри, показав, что они убивают только HER2-положительную клеточную линию. Добавление tFNA позволило большему количеству аптамера связываться с HER2, чем без tFNA, что привело к снижению уровня HER2 на клеточных поверхностях.
Хотя наноробот гораздо проще и дешевле в изготовлении, чем моноклональные антитела, пока он нуждается в дальнейшем улучшении, прежде чем его можно будет использовать для лечения рака молочной железы в клинике, говорят исследователи.
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b01320
Чтобы выяснить это, команда разработала нанороботы ДНК, состоящие из тФНК с прикрепленным аптамером HER2. При введении мышам нанороботы сохранялись в кровотоке более чем в два раза дольше, чем свободный аптамер. Затем исследователи добавили нанороботов к трем клеточным линиям рака молочной железы в чашках Петри, показав, что они убивают только HER2-положительную клеточную линию. Добавление тФНК позволило большему количеству аптамера связываться с HER2, чем без тФНК, что привело к снижению уровня HER2 на клеточных поверхностях. Хотя наноробот гораздо проще и дешевле в изготовлении, чем моноклональные антитела, он, вероятно, нуждается в дальнейшем улучшении, прежде чем его можно будет использовать для лечения рака молочной железы в клинике, говорят исследователи.